作为全球高发的慢性疾病,糖尿病正困扰着数亿人群。我国患者数量已突破1 亿,且呈年轻化趋势,其中 2 型糖尿病占比超 90%,1 型糖尿病虽占比低,但对患者生活的影响更为深远。两种分型的发病机制、症状表现差异显著,也决定了不同的治疗路径。
先分清:1型与2型糖尿病,核心差异在哪?
很多人对糖尿病的认知仅停留在“控糖”,但1型与2型本质是两种不同疾病,治疗需求也天差地别。
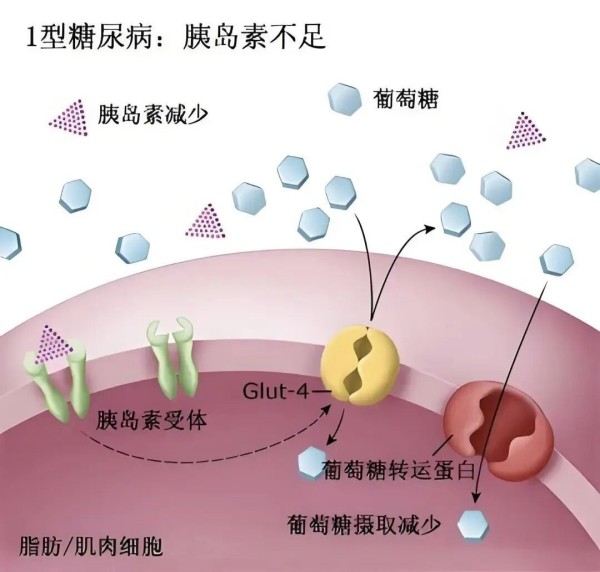
1型糖尿病:胰岛功能“完全罢工”
多在青少年时期发病,核心病因是自身免疫系统紊乱,错误攻击并破坏胰腺内负责分泌胰岛素的β细胞,导致胰岛素完全缺乏。患者发病急、症状重,常伴随多饮、多食、多尿、体重骤降,需终身依赖外源性胰岛素注射维持生命。而IPS 细胞技术的出现,为这类患者带来了摆脱终身依赖的全新希望。
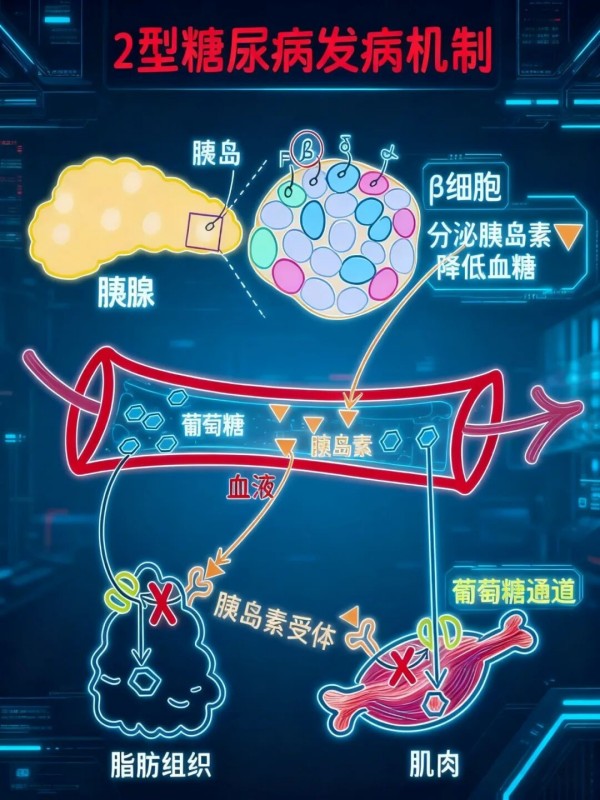
2型糖尿病:胰岛素“抵抗或分泌不足”
多在中老年时期发病,与肥胖、遗传、不良生活习惯密切相关。患者胰腺仍有一定β细胞功能,能分泌胰岛素,但身体组织对胰岛素不敏感(即“胰岛素抵抗”),或胰岛素分泌量无法满足需求,导致血糖升高。发病初期症状隐匿,部分患者可通过饮食控制、运动或口服降糖药控制血糖,后期可能需要胰岛素辅助治疗,并发症以心血管疾病、神经病变更为常见。
传统治疗:能“控糖”却难“根治”
目前临床主流治疗手段,核心目标是控制血糖水平,延缓并发症发生,但均无法从根源上修复受损的胰岛功能。
1型糖尿病:依赖胰岛素注射或胰岛素泵持续输注,需频繁监测血糖、调整剂量,患者生活质量受影响,且长期注射仍可能出现血糖波动。
2型糖尿病:从饮食运动干预、口服降糖药,到后期胰岛素补充,虽能逐步调整方案,但随着胰岛功能逐渐衰退,治疗效果会逐年下降,并发症风险仍无法完全规避。
这种“被动控糖”的困境,让干细胞技术成为糖尿病治疗的“破局方向”——它旨在通过再生修复能力,从根源上改善或重建胰岛功能,实现从“控糖”到“治糖”的跨越。
干细胞治疗:两大技术,针对性破解不同分型
目前干细胞治疗糖尿病的核心路径有两条,分别对应1型和2型糖尿病的病理需求,发展阶段和应用场景差异明显。
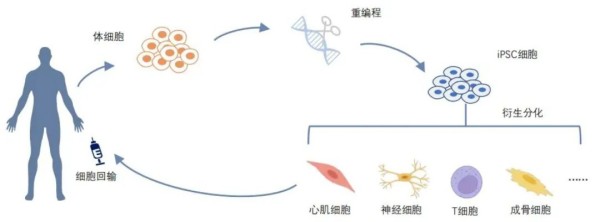
IPS细胞:1型糖尿病的“治愈曙光”,科研攻坚稳步推进
IPS细胞全称为诱导多能干细胞,通过重编程技术将皮肤、血液等体细胞转化为具有多向分化潜能的干细胞,再定向诱导为能分泌胰岛素的胰岛β细胞。其核心目标是为1型糖尿病患者“重建胰岛功能”,理论上可实现摆脱终身胰岛素依赖的愿景。这无疑为1型糖尿病患者带来了前所未有的希望。
目前,全球已有多个成功案例,部分患者通过该治疗实现了长期不依赖胰岛素的目标,这些案例不仅验证了技术的可行性,更给广大1型糖尿病患者注入了信心。当下,科研人员正围绕技术优化坚持攻坚,推动其从临床研究向规模化应用迈进,我们满心期待这项技术能早日成熟落地,让更多糖友从中获益,彻底摆脱胰岛素依赖的枷锁。
MSC细胞:适配2型糖尿病的治疗需求
MSC细胞即人脐带间充质干细胞,源自新生儿脐带组织,属于成体干细胞,具有低免疫原性、抗炎及免疫调节的核心优势,更适合2型糖尿病的治疗需求——无需重建胰岛功能,而是通过改善胰岛素抵抗、保护残存β细胞,实现血糖的稳定控制。
凭借其独特的治疗优势,MSC细胞为2型糖尿病患者提供了全新的治疗选择,具体亮点如下:
l 无免疫排斥困扰:天然具备免疫调节功能,移植后无需使用抗排异药物,安全性更高;
l 临床验证充分:大量临床试验证实,可有效改善血糖控制、减少胰岛素或口服药用量,对肥胖相关2型糖尿病效果尤为显著,且无致瘤、致畸风险;
l 适用范围广:不仅能用于2型糖尿病的常规治疗,还可干预糖尿病肾病、神经病变等并发症,同时脐带来源丰富、制备工艺成熟,具备规模化应用潜力;
l 给药便捷:通过静脉输注即可实现全身递送,创伤小、操作简单,患者接受度高。
未来展望:技术协同,让糖尿病治疗更精准
IPS 与 MSC 两大技术路径并非对立,而是未来有望协同互补,覆盖更多糖尿病患者的需求。
干细胞技术以根源性修复能力,为糖尿病治疗带来革命性突破,更以明确的技术潜力为全球数亿糖尿病患者点亮希望,助力“摆脱控糖枷锁”的目标真正落地。